AFFRESCO PARTE 5 – LO SPEGNIMENTO DELLA CALCE
Molti anni fa avevamo l’abitudine di occuparci personalmente dello spegnimento della calce viva al fine di ottenere un grassello stagionato di alta qualità da utilizzare per il restauro di affreschi e intonaci antichi. Questa nostra particolarissima attenzione alla materia prima da utilizzare in cantiere non deve essere intesa solo come una maniacale applicazione al mestiere; la verità è che in quegli anni a cavallo fra gli ’80 e i ’90 del secolo scorso non esisteva sul mercato un grassello di calce adatto allo scopo. Le antiche cave e fornaci artigianali del nostro territorio andavano di giorno in giorno chiudendo e i prodotti messi in commercio dalla grande industria non rispondevano alla compatibilità chimico-fisica dei substrati tradizionali sia come purezza di calcare utilizzato sia come metodo di lavorazione da esso subito. Il restauro era ancora un mestiere in divenire e troppo spesso restauratori improvvisati facevano uso di prodotti industriali e chimici indiscriminatamente, giustificati certamente dalla buona fede che essi riponevano nei confronti della chimica che individuavano come la strada più giusta da seguire. L’esperienza ha confermato che prodotti largamente utilizzati solo 30 anni per la salvaguardia del patrimonio artistico si sono rivelati non idonei e, anzi, spesso causa di ulteriori danni.
Quindi a quei tempi era carente la cura, l’attenzione e soprattutto la consapevolezza che abbiamo oggi per i materiali da utilizzarsi. Questo dato di fatto non incentivava l’industria a una produzione mirata al restauro e chi operava nel campo, in modo appassionato e con cognizione, si doveva un po’ arrangiare coi propri mezzi. Ecco perché ci premurammo di realizzare un nostro grassello di calce stagionato.
Per fare ciò ci procuravamo la calce viva (abbiamo evitato la cottura dei calcari, procedimento decisamente troppo complesso e che richiedeva attrezzature adeguate) andando alla ricerca di qualche cava tra quelle poche rimaste ancora aperte nel comasco. Ancor oggi mi domando cosa devono aver pensato gli addetti ai lavori quando arrivavamo in cava con la nostra auto carica di secchi da riempire di calce viva; sicuramente ci devono aver trovato un po’ strambi e immagino anche si siano fatti un sacco di risate. Una volta capitò che caricammo un secchio un po’ bagnato. Appena riempito di calce viva questa iniziò il suo processo di idratazione, crepitando e fumando all’interno dell’abitacolo.
Quindi a quei tempi era carente la cura, l’attenzione e soprattutto la consapevolezza che abbiamo oggi per i materiali da utilizzarsi. Questo dato di fatto non incentivava l’industria a una produzione mirata al restauro e chi operava nel campo, in modo appassionato e con cognizione, si doveva un po’ arrangiare coi propri mezzi. Ecco perché ci premurammo di realizzare un nostro grassello di calce stagionato.
Per fare ciò ci procuravamo la calce viva (abbiamo evitato la cottura dei calcari, procedimento decisamente troppo complesso e che richiedeva attrezzature adeguate) andando alla ricerca di qualche cava tra quelle poche rimaste ancora aperte nel comasco. Ancor oggi mi domando cosa devono aver pensato gli addetti ai lavori quando arrivavamo in cava con la nostra auto carica di secchi da riempire di calce viva; sicuramente ci devono aver trovato un po’ strambi e immagino anche si siano fatti un sacco di risate. Una volta capitò che caricammo un secchio un po’ bagnato. Appena riempito di calce viva questa iniziò il suo processo di idratazione, crepitando e fumando all’interno dell’abitacolo.
Dovemmo percorrere tutto il tragitto fino a Varese a finestrini completamente abbassati. Il calore che questa reazione innesca è talmente alto che il secchio di plastica si corrose. Comunque una volta portata a casa la materia prima procedevamo allo spegnimento per innaffiatura, lentamente e gradualmente, rimestando continuamente per attivare il processo in modo costante su tutto il materiale. Non si trattava di un’operazione facile. Il calore e i fumi che si diffondevano erano non solo fastidiosi ma anche pericolosi e dovevamo premunirci di adeguati indumenti, mascherine e guanti, per non esserne investiti. A questo punto, quando la calce viva aveva smesso di scoppiettare e fumigare e tutto il materiale si era trasformato in pasta, la fase di spegnimento si poteva dire conclusa. Il grassello di calce così ricavato era pronto per essere messo a stagionare.
Abbiamo utilizzato questo grassello per molti anni finché finalmente non iniziammo a trovare in commercio ottimi prodotti pensati e realizzati per il restauro.
Ma adesso analizziamo più da vicino il processo di spegnimento della calce.
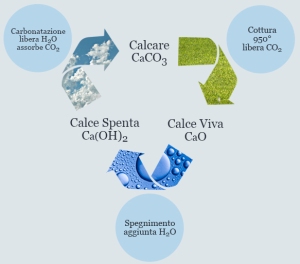
Nel capitolo precedente abbiamo seguito i primi passaggi per la realizzazione della calce in quello che viene definito “il ciclo della calce”, e precisamentel’estrazione e la cottura della roccia calcarea.
Durante il processo di cottura il minerale proveniente dalla cava, carbonato di calcio (calcare, CaO3), sottoposto a una prefissata quantità di calore (900° C), si trasforma in ossido di calcio (calce viva, CaO) e si libera di anidride carbonica (CO2). La reazione è endotermica e necessita pertanto per svilupparsi di un apporto calorico ottenuto tramite l’utilizzo di un combustibile.
Schematizzato chimicamente si traduce in questa formula:
CaCO3 -> CaO + CO2
Prima di essere utilizzata in edilizia la calce viva deve subire un ennesimo processo, detto di spegnimento o idratazione, attraverso il quale l’ossido di calcio (CaO) si trasforma in idrossido di calce (Ca(OH)2), calce spenta o calce idrata.
Il processo è riassunto nella seguente formula:
CaO + H2O -> Ca(OH)2
La reazione è fortemente esotermica (sviluppo di calore) e, in relazione alla quantità d’acqua messa a contatto con un determinato quantitativo di calce, determina la formazione di calce idrata in polvere o calce idrata in pasta (grassello).
La polvere si ottiene quando le proporzioni tra calce e acqua sono, per così dire, “stechiometriche” (teoricamente 1Kg di CaO reagisce con 0,32kg di H2O per dare 1,32kg di Ca(OH)2), mentre il grassello o meglio la pasta di calce idrata si ha quando l’acqua è aggiunta in eccesso rispetto a quella strettamente necessaria a fare completare la reazione di trasformazione di tutto l’ossido in idrossido.
La polvere si ottiene quando le proporzioni tra calce e acqua sono, per così dire, “stechiometriche” (teoricamente 1Kg di CaO reagisce con 0,32kg di H2O per dare 1,32kg di Ca(OH)2), mentre il grassello o meglio la pasta di calce idrata si ha quando l’acqua è aggiunta in eccesso rispetto a quella strettamente necessaria a fare completare la reazione di trasformazione di tutto l’ossido in idrossido.
La modalità di spegnimento non determina soltanto la forma fisica della calce spenta (polvere o pasta) ma anche e soprattutto la qualità del prodotto finale.
A questo proposito L. B. Alberti in “De re aedificatoria” – (ca.1450) dice:
“…. non dare alla calce viva gran copia d’acqua a un tratto, poichè bisogna che si spenga a poco a poco bagnandola e ribagnandola più volte infino a tanto che al certo se ne sia imbibita; di poi in luogo anzichenò umidetto et all’ombra, senza mescolarvi cosa alcuna si deve serbare stietta, coperta solamente di sopra con poca rena, infino a tanto che per la lunghezza di tempo più liquidamente si lieviti….”.
Anche il Palladio ne “I Quattro Libri dell’Architettura”, parlando dello spegnimento della calce conferma le nozioni tecniche dell’Alberti:
‘…cotta si deue bagnare, e non infondere in una volta tutta l’acqua, ma in fiate, continuamente però, acciò che non si abbruci, fin ch’ella sia ben stemperata. Di poi si riponga in luogo humido e nell’ombra, senza mescolarui cosa alcuna, solamente di leggera sabbia coprendola e quanto sarà più macerata, tanto sarà più tenace, e migliore…’.
Da queste indicazioni degli antichi maestri si trae l’inevitabile conclusione che, per la riuscita di un’ottima calce, è indispensabile controllare l’operazione di spegnimento aggiungendo alla calce viva poca acqua per volta. Agendo in questo modo si mantiene sotto controllo la temperatura a cui avviene la reazione. Al di sotto dei 100°C (precisamente tra 70 e 85°C) si ottiene la calce idrata migliore, con particelle di idrossido di calcio piccole e di grande superficie specifica. Controllando costantemente il rapporto calce viva/acqua di spegnimento l’idratazione potrà avvenire ad una temperatura ottimale e costante durante tutto il processo. La temperatura, oltre che con il giusto apporto di acqua in (termini di quantità), si controlla anche con la modalità di somministrazione dell’acqua stessa e con l’agitazione costante della calce in fase di spegnimento. Infine, non meno importante, in fase di idratazione è necessario verificare la qualità dell’acqua utilizzata e la sua temperatura. L’acqua non dovrà contenere solfati (sopra 500mg/l) e non dovrà essere troppo fredda, pena un ritardo nell’idratazione. Altre sostanze disciolte nell’acqua come ad esempio cloruri e zucchero, possono viceversa favorire il processo (ma solo in determinate concentrazioni).
Vi sono due modi per spegnere la calce viva: per immersione o per innaffiamento.
Con il primo metodo la calce viva, frantumata in blocchi delle dimensioni di una noce e sostenuta in cestelli di ferro, viene immersa per pochi istanti (circa mezzo minuto) in un recipiente colmo d’acqua. L’estrazione avviene quindi nel pieno della reazione di idratazione. A questo punto la si distende su di un piano asciutto e la si lascia riposare finché la calce si sarà ridotta in polvere e sarà pronta per essere ulteriormente pestata per renderla impalpabile e così conservata.
Con il metodo dell’innaffiamento invece si procede allo spegnimento ponendo la calce viva in apposite vasche, di legno o di muratura (dette Bagnoli), ove sarà innaffiata a poco a poco con acqua rimestando fino a che tutta la massa sfiorirà trasformandosi in poltiglia (grassello).
Se si aggiunge altra acqua a questo grassello, fino a formare uno sciroppo denso, si ottiene il “latte di calce” (1). Aggiungendo ancora acqua si ottiene l’acqua di calce (2).
Il grassello così ottenuto viene filtrato attraverso un setaccio per fermare i grumi non cotti e le forme più grossolane e poi rilasciato cadere in fosse scavate nel terreno (Calcinaie). Qui resterà a lungo a stagionare ricoperto da sabbia per ridurre il contatto con l’aria e la susseguente formazione di carbonato. La stagionatura è un’operazione importante e delicata, che deve garantire la totale idratazione degli ossidi presenti nella calce. Nel caso in cui l’idratazione, durante la stagionatura, è incompleta, essa continua quando il materiale è in opera provocando rigonfiamenti localizzati. Questi difetti, noti come calcinaroli o bottaccoli, sono tipici degli intonaci realizzati con calce aerea non perfettamente spenta.
Per capire quanto buona sia la calcina si deve osservare la sua resa in grassello, ovvero considerando il volume della pasta che si ottiene quando un dato peso di calce viva viene spento completamente con l’acqua. E’ una prova che si esegue attendendo che il grassello abbia assorbito tutta l’acqua che può e asciugandosi lascia vedere le prime fessure sulla superficie.
Il saggio ci consente di distinguere le calcine grasse da quelle magre.
Le calcine grasse mostrano un forte rigonfiamento allo spegnimento; sono avidissime di acqua e sono molto bianche, pastose ed untuose al tatto; ovviamente sono quelle più adatte per essere usate in campo artistico sia per dipingere che per restaurare anche gli intonaci antichi.
Le calcine magre chiedono minor acqua, si gonfiano poco, sono poco pastose ed emanano minor fumo durante lo spegnimento.
Un chilo di calcina viva grassa fornisce da 1,8 a 2,5 litri di grassello assumendo da 1,7 a 2,8 litri d’acqua.
Un chilo di calcina viva magra fornisce da 1,4 a 1,8 litri di grassello ed assume solamente da 1,0 a 1,7 litri d’acqua. (3)Le impurità presenti nella calce sono responsabili della magrezza dei grasselli prodotti. Per la maggior parte la presenza dell’Ossido di Magnesio che assumendo acqua non rigonfia. Oltre allo spegnimento la stessa cottura risulta difficoltosa in presenza di impurità del calcare originale che necessita una cottura a temperature elevatissime.
Il saggio ci consente di distinguere le calcine grasse da quelle magre.
Le calcine grasse mostrano un forte rigonfiamento allo spegnimento; sono avidissime di acqua e sono molto bianche, pastose ed untuose al tatto; ovviamente sono quelle più adatte per essere usate in campo artistico sia per dipingere che per restaurare anche gli intonaci antichi.
Le calcine magre chiedono minor acqua, si gonfiano poco, sono poco pastose ed emanano minor fumo durante lo spegnimento.
Un chilo di calcina viva grassa fornisce da 1,8 a 2,5 litri di grassello assumendo da 1,7 a 2,8 litri d’acqua.
Un chilo di calcina viva magra fornisce da 1,4 a 1,8 litri di grassello ed assume solamente da 1,0 a 1,7 litri d’acqua. (3)Le impurità presenti nella calce sono responsabili della magrezza dei grasselli prodotti. Per la maggior parte la presenza dell’Ossido di Magnesio che assumendo acqua non rigonfia. Oltre allo spegnimento la stessa cottura risulta difficoltosa in presenza di impurità del calcare originale che necessita una cottura a temperature elevatissime.
Philibert de l’Orme nei suoi trattati che scrisse nella prima metà del cinquecento presso la corte francese di Francesco I, ci illustra in poche sintetiche ma efficaci parole ciò che fin qui abbiamo detto:
“…..la calce è buona se è ben cotta, bianca e grassa, se non è sfiorita e se risuona battendola; se bagnata manda uno spesso fumo, e nello istemperarla si attacca alla marra. Il modo di ben istemperarla per formare un’eccellente malta, è d’ammassarne in una fossa tal quantità che farà bisogno, poi coprirla egualmente da per tutto di buona sabbia per un piede o due di altezza, poi gettarvi sopra dell’acqua perché la sabbia ne sia ben inzuppata, e la calce che rimane al di sotto possa fondersi e sciogliersi senza abbruciare, il che accadrebbe se non le si desse acqua in sufficiente quantità. Se si vedesse la sabbia aprirsi in qualche luogo, e dar passaggio al fumo, bisogna subito ricoprire le fessure. Con questa preparazione la calce si cambierà, corso un tempo conveniente, in un pastone grasso tanto e untuoso, che a mala pena si potrà cavarne la pialla, e produrrà una malta d’ottima qualità per la intonacatura dei muri e pei lavori di stucco.”
Fin qui abbiamo avuto modo di conoscere la calce idrata in polvere e il grassello. In commercio si può trovare anche la calce idrata in pasta che potrebbe indurre in confusione pensando ad essa come una sorta di grassello. In verità la calce idrata in pasta e il grassello di calce sono prodotti molto diversi l’uno dall’altro e non andrebbero mai confusi! La loro principale differenza è che la prima non beneficia degli straordinari effetti che il tempo produce in ordine alla struttura chimico-fisica del materiale, durante quello che viene chiamato invecchiamento o maturazione. Come abbiamo già anche visto più sopra durante l’invecchiamento (fase che caratterizza e distingue il grassello dalla pasta di calce idrata) i cristalli di idrossido di calcio (portlandite) subiscono importanti cambiamenti morfologici e dimensionali, con il risultato di aumentare plasticità, lavorabilità e ritenzione d’acqua.
Alcuni dei vantaggi ottenuti dall’impiego, nella formulazione di malte e pitture, di grassello di calce correttamente invecchiato in luogo al suo corrispettivo di calce idrata in pasta sono:
1. con il grassello di calce si ottengono malte più “grasse”, più plastiche e lavorabili, quindi meno soggette a ritiro, a suzione da parte delle murature e pertanto preferibili sul piano tecnico ed estetico;
2. le pitture formulate con grassello di calce, rispetto a quelle formulate con calce idrata in pasta (o in polvere), hanno una minor tendenza a segregare, non richiedono additivi organici, carbonatano, si fissano al supporto con maggior velocità e forza e, se ben applicate, non hanno tendenza a “spolverare”;
3. il grassello di calce si carbonata con maggiore rapidità della calce aerea in pasta (o in polvere), con benefici rispetto alla durabilità e alle resistenze dell’opera che si andrà a realizzare, sia questa una malta, un intonaco o una pittura murale ecc.
Ricapitolando
La calce aerea (il suo nome trae origine dall’attitudine a fare presa soltanto all’aria) si ottiene;
- dalla cottura dei calcari più puri (rocce ad alto contenuto di carbonati di calcio) da cui si ottiene la calce ‘viva’, costituita prevalentemente da ossido di calcio;
e
- successivo spegnimento della stessa, la calce ‘idrata’ o ‘spenta’ costituita prevalentemente da idrossido di calcio.
In relazione al metodo di spegnimento che sarà utilizzato si otterrà il grassello o la calce idrata in polvere.(4)
Calce idraulica
Oltre a quanto già detto non possiamo dimenticare di citare in questo contesto la calce idraulica (anche se non idonea per la realizzazione di un affresco) che a differenza della precedente ha la capacità di far presa e indurire anche sott’acqua.
Le prime testimonianze di uso di malte a base calce idraulica risalgono ai Greci.
Queste erano ottenute dalla miscelazione di grassello di calce e sabbie pozzolaniche ad esempio, la pietra pomice dell’isola di Santorino, macinata e mescolata all’inerte, oppure la terra vulcanica, di colore scuro, dell’isola di Thera, o ancora frammenti di laterizi pestati.
Questi ultimi due sistemi vennero particolarmente sviluppati in età romana, quando si impiegò abbondantemente la terra di origine vulcanica dei colli Albani e del golfo di Napoli, che venne detta pozzolana dalla città di Puteoli-Pozzuoli. Anche l’aggiunta di frammenti di laterizi o di altri prodotti ceramici, che conferiscono alla malta il tipico colore rossastro e che le valgono la definizione di ‘cocciopesto’, data dagli archeologi, fu molto in uso, sia per i pavimenti, sia per gli intonaci, soprattutto nelle cisterne e negli acquedotti.
Tutte queste sostanze usate come additivi sono ricche di silice e allumina attive, le quali permettono la formazione di silicati e alluminati di calcio, composti più resistenti all’acqua di quanto non sia il carbonato di calcio. (5)Una simile trasformazione chimica del calcio si poteva ottenere anche cuocendo calcare marnoso, cioè contenente argilla, al posto del calcare puro o del calcare magnesiaco; in questo caso la formazione di silicati e alluminati di calcio, che conferiscono l’idraulicità, è propria della calce stessa, e non dovuta all’aggiunta degli additivi. Calci di questo genere erano chiamate ‘selvatiche’ in Liguria (perché prodotte nelle campagne); ‘forti’ in Lombardia e vennero dette ‘idrauliche’ a partire dall’Ottocento. (6)
Oltre a quanto già detto non possiamo dimenticare di citare in questo contesto la calce idraulica (anche se non idonea per la realizzazione di un affresco) che a differenza della precedente ha la capacità di far presa e indurire anche sott’acqua.
Le prime testimonianze di uso di malte a base calce idraulica risalgono ai Greci.
Queste erano ottenute dalla miscelazione di grassello di calce e sabbie pozzolaniche ad esempio, la pietra pomice dell’isola di Santorino, macinata e mescolata all’inerte, oppure la terra vulcanica, di colore scuro, dell’isola di Thera, o ancora frammenti di laterizi pestati.
Questi ultimi due sistemi vennero particolarmente sviluppati in età romana, quando si impiegò abbondantemente la terra di origine vulcanica dei colli Albani e del golfo di Napoli, che venne detta pozzolana dalla città di Puteoli-Pozzuoli. Anche l’aggiunta di frammenti di laterizi o di altri prodotti ceramici, che conferiscono alla malta il tipico colore rossastro e che le valgono la definizione di ‘cocciopesto’, data dagli archeologi, fu molto in uso, sia per i pavimenti, sia per gli intonaci, soprattutto nelle cisterne e negli acquedotti.
Tutte queste sostanze usate come additivi sono ricche di silice e allumina attive, le quali permettono la formazione di silicati e alluminati di calcio, composti più resistenti all’acqua di quanto non sia il carbonato di calcio. (5)Una simile trasformazione chimica del calcio si poteva ottenere anche cuocendo calcare marnoso, cioè contenente argilla, al posto del calcare puro o del calcare magnesiaco; in questo caso la formazione di silicati e alluminati di calcio, che conferiscono l’idraulicità, è propria della calce stessa, e non dovuta all’aggiunta degli additivi. Calci di questo genere erano chiamate ‘selvatiche’ in Liguria (perché prodotte nelle campagne); ‘forti’ in Lombardia e vennero dette ‘idrauliche’ a partire dall’Ottocento. (6)

La produzione dei leganti idraulici iniziò in Italia nel 1856 a Palazzolo sull’Oglio, in uno stabilimento per la produzione della calce idraulica.
La particolare proprietà delle calci idrauliche naturali si ottiene dalla calcinazione di calcari contenenti dall’8 al 20% di argilla ad una temperatura di 1000-1200°C, una temperatura quindi molto superiore a quella che occorre per la cottura del calcare puro per la produzione del grassello.
Le zolle calcinate hanno una colorazione grigio-gialla e sono formate da una miscela di calcelibera e silicati, alluminati e ferriti di calcio. Anche in questo caso l’operazione di spegnimento richiede una particolare cura, in quanto da una parte deve assicurare la completa trasformazione della calce viva in idrossido, evitando che questa reazione avvenga durante la presa con conseguenti rigonfiamenti e disgregazioni della malta, dall’altra bisogna evitare che un eccesso di acqua dia luogo all’idratazione dei silicati e alluminati e ad un loro prematuro indurimento. Così facendo si ottengono zolle pulverulenti che vengono lasciate all’aria, coperte a ben stagionare.
A stagionatura terminata saranno macinate al fine di ottenere una polvere molto fine e così conservate in un luogo asciutto perché a contatto con acqua o umidità induriscono in poco tempo.
Paola Mangano
![ms. D.IX.1, AUGUSTINUS AURELIUS [SANTO], De civitate Dei Fano, 1450. - Miniature: Maestro del De civitate Dei, [anonimo maestro ferrarese]. (Sant'Agostino nello studio), c. 15r.](https://passionarte.files.wordpress.com/2014/06/15r.jpg?w=329&h=341)
ms. D.IX.1, AUGUSTINUS AURELIUS [SANTO], De civitate Dei
Fano, 1450. – Miniature: Maestro del De civitate Dei, [anonimo maestro ferrarese].
(Sant’Agostino nello studio), c. 15r.
Fano, 1450. – Miniature: Maestro del De civitate Dei, [anonimo maestro ferrarese].
(Sant’Agostino nello studio), c. 15r.
Curiosità
Calce viva e calce spenta.
4. 3. Esaminiamo anche il fenomeno sorprendente della calce. Eccettuato il caso, di cui abbiamo parlato abbastanza, che biancheggia nel fuoco, mentre in esso altre sostanze anneriscono, accoglie anche in forma molto occulta il fuoco e in una zolla fredda lo conserva così di nascosto a quelli che toccano che non si manifesta affatto ad alcun nostro senso, ma ravvisato con una esperimentazione, anche se non così manifesta, si può notare che vi persiste attutito. La chiamiamo appunto calce viva, come se il fuoco nascosto sia l’anima invisibile di un corpo visibile. Ed è un fenomeno sorprendente che quando si spegne allora si accende. Per privarla del fuoco nascosto viene immersa nell’acqua, viene inondata di acqua e, sebbene prima sia fredda, si riscalda nell’acqua, da cui tutte le cose calde sono raffreddate. Dunque come se quella zolla esali l’ultimo respiro, il fuoco, che vi era nascosto, esce fuori e la calce, come per morte avvenuta, è così fredda che con l’aggiunta dell’acqua non ribollirà. E noi consideriamo calce spenta quella che consideravamo calce viva. Sembra che si possa aggiungere qualcosa a questo fenomeno singolare? Certo che si aggiunge. Se non applichi l’acqua ma l’olio, che è di più fomite del fuoco, la calce non ribolle né cospargendola d’olio né immergendovela. Se leggessimo e udissimo questo fenomeno sorprendente in una qualche pietra indiana e non fosse possibile che esso giungesse alla nostra diretta verifica, penseremmo sicuramente a un’impostura o ce ne meraviglieremmo fortemente. Ma le costatazioni giornaliere di questi avvenimenti che accadono sotto i nostri occhi, sebbene non meno sorprendenti nella forma, perdono importanza per la frequente ripetizione. Difatti abbiamo smesso di meravigliarci di alcuni casi che fu possibile offrire alla nostra ammirazione dalla stessa India, la quale è una parte del globo lontana da noi.S. Agostino: La Città di Dio: Capp. XVII- XXII
Libro ventunesimo – LA FINALE PENA ETERNA – Non tutto è riducibile a un criterio razionale – 4.3
4. 3. Esaminiamo anche il fenomeno sorprendente della calce. Eccettuato il caso, di cui abbiamo parlato abbastanza, che biancheggia nel fuoco, mentre in esso altre sostanze anneriscono, accoglie anche in forma molto occulta il fuoco e in una zolla fredda lo conserva così di nascosto a quelli che toccano che non si manifesta affatto ad alcun nostro senso, ma ravvisato con una esperimentazione, anche se non così manifesta, si può notare che vi persiste attutito. La chiamiamo appunto calce viva, come se il fuoco nascosto sia l’anima invisibile di un corpo visibile. Ed è un fenomeno sorprendente che quando si spegne allora si accende. Per privarla del fuoco nascosto viene immersa nell’acqua, viene inondata di acqua e, sebbene prima sia fredda, si riscalda nell’acqua, da cui tutte le cose calde sono raffreddate. Dunque come se quella zolla esali l’ultimo respiro, il fuoco, che vi era nascosto, esce fuori e la calce, come per morte avvenuta, è così fredda che con l’aggiunta dell’acqua non ribollirà. E noi consideriamo calce spenta quella che consideravamo calce viva. Sembra che si possa aggiungere qualcosa a questo fenomeno singolare? Certo che si aggiunge. Se non applichi l’acqua ma l’olio, che è di più fomite del fuoco, la calce non ribolle né cospargendola d’olio né immergendovela. Se leggessimo e udissimo questo fenomeno sorprendente in una qualche pietra indiana e non fosse possibile che esso giungesse alla nostra diretta verifica, penseremmo sicuramente a un’impostura o ce ne meraviglieremmo fortemente. Ma le costatazioni giornaliere di questi avvenimenti che accadono sotto i nostri occhi, sebbene non meno sorprendenti nella forma, perdono importanza per la frequente ripetizione. Difatti abbiamo smesso di meravigliarci di alcuni casi che fu possibile offrire alla nostra ammirazione dalla stessa India, la quale è una parte del globo lontana da noi.S. Agostino: La Città di Dio: Capp. XVII- XXII
Libro ventunesimo – LA FINALE PENA ETERNA – Non tutto è riducibile a un criterio razionale – 4.3

Calce viva. I romani grandi costruttori nei mercati di Traiano
A cura di: Del Moro M. P. , Lucrezia U.
Editore: Palombi Editori
Anno: 2011
A cura di: Del Moro M. P. , Lucrezia U.
Editore: Palombi Editori
Anno: 2011
Note
(1) Il latte di calce viene adoperato sia per imbiancare che per eseguire il “falso fresco”, ossia un surrogato dell’affresco di facile attuazione. Basta passare una mano di latte di calce su un muro già intonacato e secco e dipingervi sopra con colori stemperati in acqua e calce. Pur risultando una buona pittura non possiede la solidità del vero affresco. Molte pitture etrusche e romane furono eseguite con questo metodo. Non va confuso con la così detta “calce al latte” dove al posto dell’acqua si aggiunge latte vaccino.
(2) Chiamasi acqua di calce quel liquido limpido e trasparente che viene a galleggiare nelle vasche ove la calce è stata spenta con molta acqua. In soluzione con altri elementi (colla di caseina 1p., vernice coppale 1p., unbianco d’uovo, fiele ½ p.) si usava nell’antichità per mescolarla ai colori e dipingervi su intonaci di calce ed anche di gesso. Serve anche per pulire gli affreschi e per purificare i cinabri al fine di renderli atti alla pittura ad affresco. I cinabri con questo trattamento impallidiscono ma poi non cambiano più. Se si giudica l’acqua di calce troppo forte si decanta quella che galleggia e si aggiunge nuova acqua pura.
(3) Nei moderni forni a ventilazione forzata, ove il calcare viene cotto per essere trasformato in calce viva, anche se alimentati a legna (segatura o polverino), la calce si ottiene sempre per cottura “media” (circa 1150°C) o anche “forte” (circa 1300°C) di pietrame di piccola pezzatura che, venendo a contatto con la fiamma diretta meccanicamente aspirata nell’interno della sua massa, si arroventa bruscamente, tendendo a sinterizzarsi, ossia ad essere costituita non più da singoli cristalli di ossido di calcio ma da aggregati compatti degli stessi, tanto più grossolani quanto più spinta è la cottura, determinando una diminuzione della porosità, della superficie specifica e della reattività, il che vuol dire minore capacità di idratazione e, quindi, minore resa in grassello. Il contatto diretto del materiale con la fiamma, inoltre, spesso ne compromette la bianchezza e la purezza, non essendo possibile evitare che su di esso si depositino i residui incombusti (ceneri).
(4) Dalla cottura dei calcari che contengono anche carbonato di magnesio si ottiene ancora ‘calce viva’ e successivamente ‘calce idrata’, che conterrà insieme all’ossido/idrossido di calcio, l’ossido e l’idrossido di magnesio. I termini di calce viva e calce spenta si usano, pertanto, indipendentemente dal contenuto o meno di magnesio, ma quando si vuole specificare la presenza del solo calcio, oppure del calcio e del magnesio insieme, si distinguono le ‘calci calciche’ (CL) e le ‘calci dolomitiche’ (DL).
(5) La pozzolana è infatti una terra di origine vulcanica e perciò è in larga misura costituita da silico-alluminati, così come la pomice, anch’essa di origine vulcanica. Il cocciopesto è costituito da frammenti di ceramica, derivata dalla trasformazione in seguito a cottura di minerali argillosi, che sono appunto silicati idrati di alluminio. Durante la cottura, poiché perdono l’acqua di cristallizzazione, la silice e l’allumina si trovano allo stato libero, non cristallino, e pertanto possono facilmente combinarsi col calcio.
(6) Un metodo per la preparazione di malta idraulica senza addittivi venne descritto, alla metà del XVIII secolo, dal noto ingegnere francese Loriot, appassionato studioso delle calci di età romana; egli propose un sistema per la costruzione di opere idrauliche con calce aerea, che consisteva nell’aggiungere a un grassello “spento da parecchio tempo e conservato in tutta la sua freschezza ” un terzo di calce viva in polvere. Secondo il Loriot, raggiungendo il “giusto accordo” dal quale “deriva la perfezione” , si poteva ottenere un composto con l’”eminente qualità di restare impermeabile all’acqua” .
fonte: passionarte.wordpress.com









Nessun commento:
Posta un commento